電化學│常見電池知識
瀏覽次數: 342 發布時間:2026-03-09 15:15:04 發布人:editor
一、電池的"記憶效應"
記憶效應就是電池用電未完再充電時容量下降("記住"較短的放電區間)。通俗說,就是電池長期不徹底充電、放電,易在電池內留下痕跡,降低電池容量。電池好像記憶了用戶日常的充、放電幅度和模式。氫-鎳、鎘-鎳電池的記憶效應較為嚴重,而鋰離子電池不存在記憶效應。
二、"電化學惰性"
"惰性"只是一個具有相對意義的概念。電化學惰性,通常指某種材料上進行電化學反應速率慢,該電化學反應具有較小的交換電流,電化學極化大。這個概念僅具有相對意義,例如,在金電極上很多有機小分子以及氫氣的電化學氧化性能很差,但是通過降低其粒徑并利用其特殊的表面晶面,其電催化活性可以和金屬鉑相媲美。一般認為堿錳電池正極中的黑錳礦相是電化學惰性的,不過通過摻雜NaBiO3納米顆粒后可以徹底改變其電化學活性。
三、燃料電池的基本原理
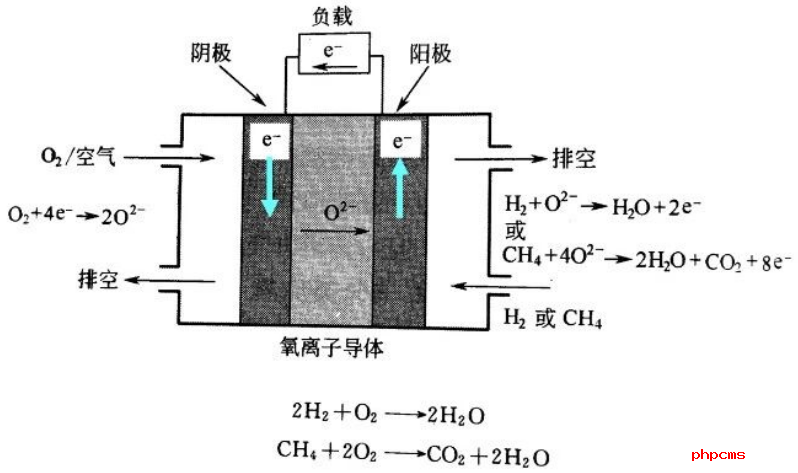
燃料電池(fuel cell)的核心部分由陽極、陰極、電解質構成。電解質通常介于陽極和陰極之間,具有傳導離子和阻止燃料和氧化劑的直接接觸的作用。陽極發生氧化反應,陰極發生還原反應。H2作為燃料被連續地輸送到陽極,在陽極電催化劑的作用下,發生電化學氧化反應(生成H+,并釋放2個自由電子)。H+通過電解質從陽極傳遞到陰極,自由電子則通過電子導體從陽極流經負載后運動到陰極。在陰極上,O2在催化劑的作用下,發生電化學還原反應,即與從電解質傳遞過來的質子和從外電路傳遞過來的電子結合生成H2O總的電池反應。兩個電極反應的電勢不同,從而產生電勢差,并釋放出電能。
四、"微電池"引起電池腐蝕
一個電化學腐蝕體系(金屬/腐蝕介質)實質上是短路的原電池,其陽極反應使金屬材料破壞,腐蝕體系中進行的氧化還原反應的化學能最終不能輸出電能,全部以熱能形式散失。這種導致金屬材料破壞的短路原電池稱為腐蝕電池。當金屬表面含有一些雜質時,金屬的電勢和雜質的電勢不盡相同,可構成以金屬和雜質為電極的許多微小的肉眼無法辨認的短路電池,稱為微電池,從而引起腐蝕。
五、電池自放電的原因及影響
一次電池或充電后的二次電池在一定條件(溫度、濕度等)下貯存時容量會有所下降,這稱為電池的自放電。一般認為電池自放電主要是由負極腐蝕和正極自放電引起的。負極腐蝕:負極多為活潑金屬,其標準電極電位比氫電極負,特別是有正電性金屬雜質存在時,雜質與負極形成腐蝕微電池。正極自放電:正極上發生副反應時,消耗正極活性物質,使電池容量下降。例如,鉛酸蓄電池正極PbO2和板柵鉛的反應,消耗部分活性PbO2。電池自放電與電池的貯存性能密切相關。作為化學電源,要求它在使用時能夠輸出電能,貯存時最好不要有能量損失。而電池存在的自放電(其大小可用自放電率表示),將直接影響電池的貯存性能。
六、金屬-空氣電池又稱"半燃料電池"
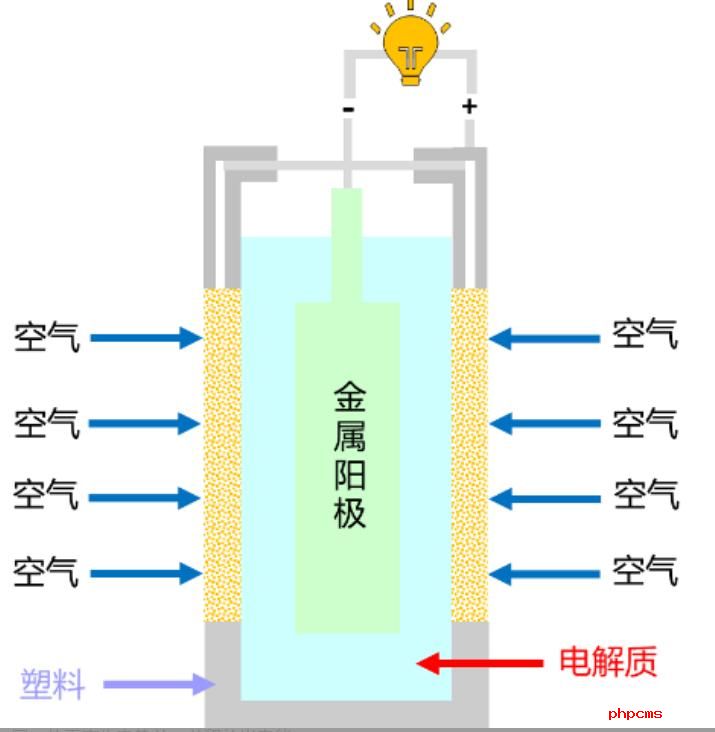
金屬-空氣電池(MAB)的特征是還原劑(如Zn、Cd等)和氧化劑(如MnO2,AgO等)分別制成負極和正極材料置于電池殼體內,放電時這些電極活性材料發生電化學氧化還原反應而不斷被消耗,待其消耗殆盡時,電池則不能再放電。MAB 的陽極材料(通常為電化學氧化活性高的活潑金屬),如 Al、Mg等在電池放電過程中被消耗;陰極具有燃料電池的特征,即氧化劑(如O2、H2O2等)從外部連續地輸送到陰極,陰極 本身不消耗。因此,將這種特征介于電池和燃料電池之間的電化學能量轉換裝置也稱為"半"燃料電池。
七、鋁作為陽極會有什么問題,如何解決?
鋁作為電池的陽極材料在實際應用中也存在一些不容忽視的問題。鋁的表面易生成一層致密的氧化物構成的鈍化膜,使鋁的氧化變得困難,負極出現很大的電化學極化,導致電極電勢達不到應有的理論電極電位,同時還造成放電時的電壓滯后現象。其次,鋁是典型的兩性金屬,活潑性較高,氧化膜一旦被破壞就會迅速發生自放電腐蝕,損失電化學容量的同時放出大量氫氣,降低電極的利用率,并影響電池正常工作。鋁表面的鈍化層是決定鋁負極性能的關鍵因素,鈍化層太厚則會降低鋁的放電速率,電化學極化增大;鈍化層太薄則鋁容易發生自放電腐蝕,導致容量損失。 解決此問題,可采用以下方法:
① 向鋁電極中添加一些微量合金元素使鋁合金化,利用元素摻雜改變鈍化層的性質,可實現"活化"和"緩蝕"目的。② 在堿性電解質中添加CaO、ZnO等可有效抑制鋁的腐蝕,減小其電化學極化。
記憶效應就是電池用電未完再充電時容量下降("記住"較短的放電區間)。通俗說,就是電池長期不徹底充電、放電,易在電池內留下痕跡,降低電池容量。電池好像記憶了用戶日常的充、放電幅度和模式。氫-鎳、鎘-鎳電池的記憶效應較為嚴重,而鋰離子電池不存在記憶效應。
二、"電化學惰性"
"惰性"只是一個具有相對意義的概念。電化學惰性,通常指某種材料上進行電化學反應速率慢,該電化學反應具有較小的交換電流,電化學極化大。這個概念僅具有相對意義,例如,在金電極上很多有機小分子以及氫氣的電化學氧化性能很差,但是通過降低其粒徑并利用其特殊的表面晶面,其電催化活性可以和金屬鉑相媲美。一般認為堿錳電池正極中的黑錳礦相是電化學惰性的,不過通過摻雜NaBiO3納米顆粒后可以徹底改變其電化學活性。
三、燃料電池的基本原理
燃料電池(fuel cell)的核心部分由陽極、陰極、電解質構成。電解質通常介于陽極和陰極之間,具有傳導離子和阻止燃料和氧化劑的直接接觸的作用。陽極發生氧化反應,陰極發生還原反應。H2作為燃料被連續地輸送到陽極,在陽極電催化劑的作用下,發生電化學氧化反應(生成H+,并釋放2個自由電子)。H+通過電解質從陽極傳遞到陰極,自由電子則通過電子導體從陽極流經負載后運動到陰極。在陰極上,O2在催化劑的作用下,發生電化學還原反應,即與從電解質傳遞過來的質子和從外電路傳遞過來的電子結合生成H2O總的電池反應。兩個電極反應的電勢不同,從而產生電勢差,并釋放出電能。

四、"微電池"引起電池腐蝕
一個電化學腐蝕體系(金屬/腐蝕介質)實質上是短路的原電池,其陽極反應使金屬材料破壞,腐蝕體系中進行的氧化還原反應的化學能最終不能輸出電能,全部以熱能形式散失。這種導致金屬材料破壞的短路原電池稱為腐蝕電池。當金屬表面含有一些雜質時,金屬的電勢和雜質的電勢不盡相同,可構成以金屬和雜質為電極的許多微小的肉眼無法辨認的短路電池,稱為微電池,從而引起腐蝕。
五、電池自放電的原因及影響
一次電池或充電后的二次電池在一定條件(溫度、濕度等)下貯存時容量會有所下降,這稱為電池的自放電。一般認為電池自放電主要是由負極腐蝕和正極自放電引起的。負極腐蝕:負極多為活潑金屬,其標準電極電位比氫電極負,特別是有正電性金屬雜質存在時,雜質與負極形成腐蝕微電池。正極自放電:正極上發生副反應時,消耗正極活性物質,使電池容量下降。例如,鉛酸蓄電池正極PbO2和板柵鉛的反應,消耗部分活性PbO2。電池自放電與電池的貯存性能密切相關。作為化學電源,要求它在使用時能夠輸出電能,貯存時最好不要有能量損失。而電池存在的自放電(其大小可用自放電率表示),將直接影響電池的貯存性能。
六、金屬-空氣電池又稱"半燃料電池"
金屬-空氣電池(MAB)的特征是還原劑(如Zn、Cd等)和氧化劑(如MnO2,AgO等)分別制成負極和正極材料置于電池殼體內,放電時這些電極活性材料發生電化學氧化還原反應而不斷被消耗,待其消耗殆盡時,電池則不能再放電。MAB 的陽極材料(通常為電化學氧化活性高的活潑金屬),如 Al、Mg等在電池放電過程中被消耗;陰極具有燃料電池的特征,即氧化劑(如O2、H2O2等)從外部連續地輸送到陰極,陰極 本身不消耗。因此,將這種特征介于電池和燃料電池之間的電化學能量轉換裝置也稱為"半"燃料電池。

七、鋁作為陽極會有什么問題,如何解決?
鋁作為電池的陽極材料在實際應用中也存在一些不容忽視的問題。鋁的表面易生成一層致密的氧化物構成的鈍化膜,使鋁的氧化變得困難,負極出現很大的電化學極化,導致電極電勢達不到應有的理論電極電位,同時還造成放電時的電壓滯后現象。其次,鋁是典型的兩性金屬,活潑性較高,氧化膜一旦被破壞就會迅速發生自放電腐蝕,損失電化學容量的同時放出大量氫氣,降低電極的利用率,并影響電池正常工作。鋁表面的鈍化層是決定鋁負極性能的關鍵因素,鈍化層太厚則會降低鋁的放電速率,電化學極化增大;鈍化層太薄則鋁容易發生自放電腐蝕,導致容量損失。 解決此問題,可采用以下方法:
① 向鋁電極中添加一些微量合金元素使鋁合金化,利用元素摻雜改變鈍化層的性質,可實現"活化"和"緩蝕"目的。② 在堿性電解質中添加CaO、ZnO等可有效抑制鋁的腐蝕,減小其電化學極化。
